牙周炎作为全球范围内常见的慢性炎症性疾病之一,不仅是导致成年人牙齿丧失的主要原因,其引起的持续性炎症与牙槽骨进行性破坏,也与糖尿病、心血管疾病等全身性疾病的发生发展密切相关。临床常见的治疗手段如刮治、抗生素应用等,往往难以在有效控制炎症的同时,同步实现牙槽骨这一矿化组织的结构性再生。
近年来,利用生物电信号调控组织再生成为一个备受关注的新方向。研究表明,局部微电场可有效调节细胞行为,尤其在炎症微环境下依然具备促进骨修复的潜力。然而,如何在动态、湿润且伴有病原微生物干扰的口腔环境中,实现稳定电信号生成与传导、免疫调节及成骨分化之间的协同耦合,是相关生物材料研发面临的核心瓶颈。

近日,复旦大学附属口腔医院韦晓玲主任团队与复旦大学未来信息创新学院张荣君教授团队开展医工交叉团队合作,在该领域取得了重要进展。团队创新提出了一种 “异质结增强压电效应”与“双盐协同仿生调控” 的一体化策略,构建出一种可用于牙周炎微创注射治疗的多功能压电水凝胶(POG-HC)。该材料在体内外均展现出优异的免疫调节/成骨再生能力。相关研究以《Dual-Strategy Design of Heterojunction-Enhanced Piezoelectric Hydrogels for Periodontitis Treatment》为题,发表于国际知名期刊《Advanced Science》。复旦大学附属口腔医院的周强强医师、李昌忆医师与复旦大学未来信息创新学院的方绍钧博士为本文的共同第一作者,韦晓玲主任和张荣君教授为共同通讯作者。
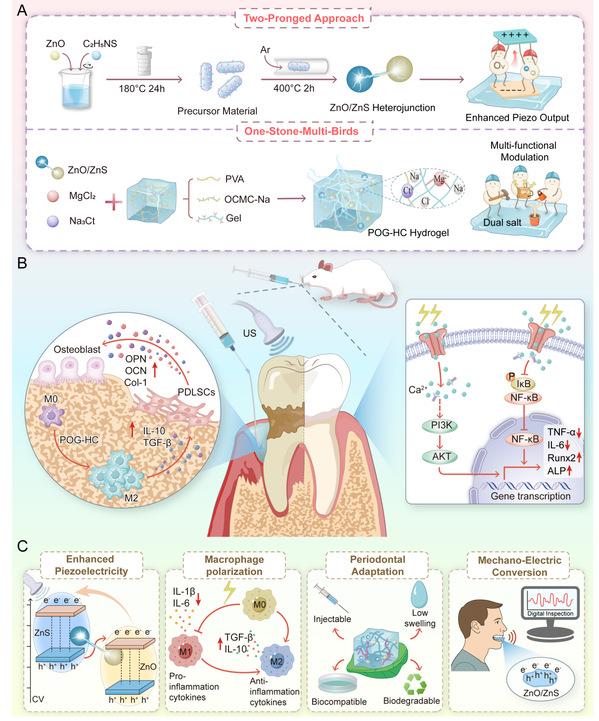
图1. 集成双策略设计的压电水凝胶用于牙周炎治疗的示意图。
研究的创新在于其双策略协同设计理念,有效克服了传统压电材料在生物环境下输出弱、传导效率低、功能单一难以匹配牙周环境等问题。团队首先原位构建ZnO/ZnS异质结并引入氧空位缺陷,形成高效内建电场,使材料在超声等机械刺激下电荷分离与迁移能力显著增强,为牙周组织微环境中产生稳定治疗性微电场奠定基础。同时,通过引入氯化镁(MgCl₂)与柠檬酸三钠(Na₃Ct)双盐体系至聚乙烯醇(PVA)基多网络水凝胶中,赋予材料较高的离子电导率(≈3.82 mS·cm⁻¹)与良好的电响应稳定性。基于该设计,POG-HC水凝胶在湿润条件下仍保持灵敏电响应,可于超声激发下稳定输出约150 mV电压,并在体外同步促进人牙周膜干细胞成骨分化及巨噬细胞向M2表型极化,通过免疫重塑有效缓解干细胞炎症负荷,展现出电生理调控、免疫调节与成骨促进的协同治疗效应。
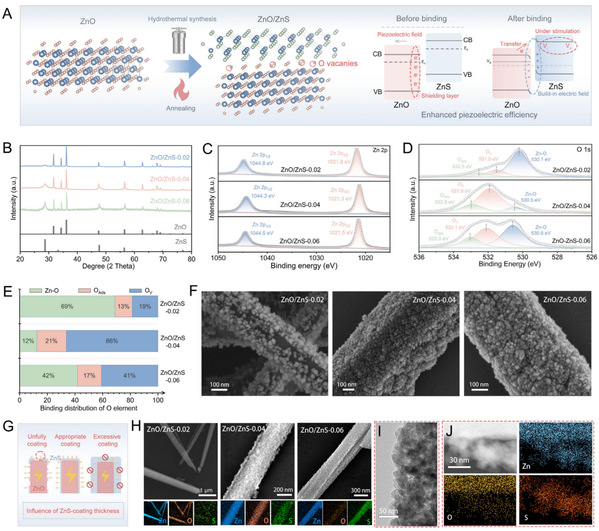
图2. ZnO/ZnS异质结的构建与压电性能表征。
此外,研究团队通过转录组测序和分子生物学实验,深入解析了该材料的作用机制。研究发现,其促成骨效应的核心是启动了一个由“超声-压电信号-钙离子通路-多通路协同”构成的精密级联反应,最终重塑 PDLSCs 的表型程序并促进成骨分化。
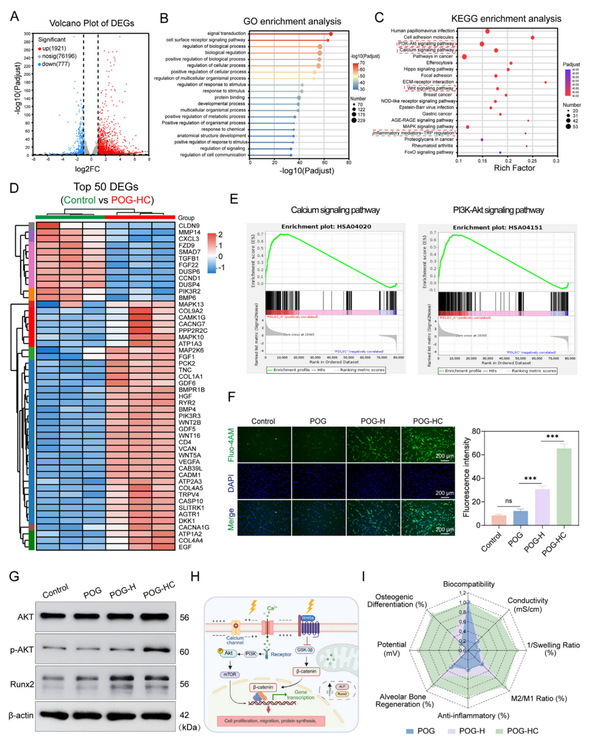
图3. 转录组测序揭示POG-HC压电水凝胶治疗牙周炎的潜在作用机制。
综上,这项工作为炎症性骨缺损的再生修复提供了一种全新的电生理治疗策略,具有广阔的临床转化前景。同时,其设计理念也为开发用于其他组织(如骨、软骨、神经)再生修复的下一代智能生物材料提供了重要借鉴。
文章链接:https://doi.org/10.1002/advs.202600017

 复旦主页
复旦主页 实验室安全
实验室安全 复旦邮箱
复旦邮箱 办事大厅
办事大厅

